關於樂和
乐于心,和与众,与己乐,与人和; 心宽念纯,百病无生。

如果問結直腸癌患者最怕甚麼?肝轉移一定名列前茅,研究表明,肝轉移是結直腸癌患者最主要的死亡原因[1-2]。今天我們通過一個真實案例來揭開結直腸癌的致命真相,請提前防範!
2024年1月,李先生因為便血在北京某三甲醫院做了腸鏡檢查,看到距肛門約12cm處存在腫物,等到活檢結果出來,確診是直腸中分化腺癌。
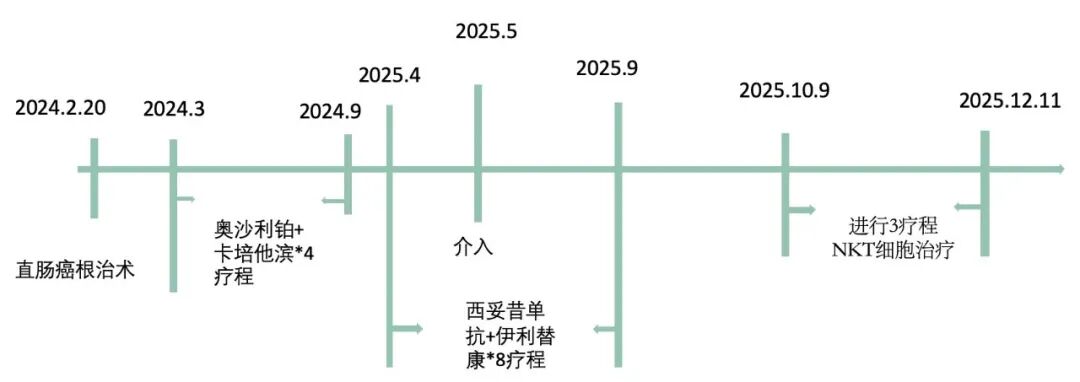
確診後,李先生的家人趕緊跑醫院、找醫生,在2024年2月做了直腸癌根治術。
術後病理顯示腫瘤最大直徑2.5cm,侵及固有肌層,脈管侵犯陽性,淋巴結轉移(2/13),分期為pT2N1bMx。免疫組化顯示錯配修復蛋白表達完整,Her-2陰性。
手術後2024年3月進入輔助化療,先是做了4療程奧沙利鉑+卡培他濱,後續又做了4療程單藥卡培他濱,直到2024年9月底完成化療。
手術切了腫瘤,又做了8個療程全身化療,術後CEA持續正常維持在1.7ng/ml左右,李先生覺得體內的癌細胞殺得很乾淨,應該沒甚麼問題了。
但是反轉來得猝不及防,2025年3月術後13個月復查竟然出現了肝轉移。
肝臟可以說是結直腸癌血行轉移最愛去的靶器官,由於結腸和直腸大部分的血液經門靜脈直接流至肝臟,肝臟的肝竇結構會讓血流速度減慢,就給了癌細胞容易在此滯留的機會,再加上肝臟微環境適宜癌細胞生存等因素,讓肝臟被結直腸癌“偏愛”。
15%~25%結直腸癌患者在確診時即合併有肝轉移,而另15%~25%的患者在結直腸癌原發灶根治術後發生肝轉移[3]。
很多人一聽“肝轉移”就以為癌症到了晚期沒救了,先別緊張,對於結直腸癌來說,肝轉移是一個特殊的存在。
80%~90%的肝轉移灶初始無法獲得根治性切除[3],李先生的情況也是如此。但研究表明,最初肝轉移灶無法根除的患者經治療後可以轉化為可切除或消融。肝轉移灶能完全切除或消融後,患者的中位生存期達35~60個月,5年總體生存率可達40%~57%[4-8]。
於是2025年4月李先生開始二線化療,8療程的西妥昔單抗+伊利替康。
期間2025年5月還對肝轉移病灶做了微波消融治療。
經過一系列治療,李先生的腫瘤標誌物CEA基本穩定下來,影像學顯示肝內病灶控制,無新發灶。但是CA19-9和細胞角蛋白19片段出現波動升高。
CA19-9的波動升高,由於肝臟是CA19-9代謝和清除的重要器官,有肝轉移病史的患者出現這一指標的升高常被視為肝內病灶活動或進展的間接信號。
細胞角蛋白19片段波動升高,治療後這一指標升高可能反映殘留腫瘤細胞活躍或微轉移灶存在,如果持續或進行性升高則提示疾病可能進展。
兩者同時波動升高,要高度警惕是不是有隱匿性腫瘤殘留或早期復發,雖然影像學上還沒有看到,但標誌物已經先一步有了變化。
① 系統藥物治療:化療+靶向藥
② 局部根治手段:微創消融或手術
③ 後續鞏固:監測+維持治療
李先生①②步治療已完成,影像檢查上看起來“乾淨了”,但是腫瘤標誌物CA19-9和細胞角蛋白19片段仍在提示微小殘留病灶的高風險,依然讓人沒辦法安心。
後續該如何維持現有的治療成果,清除殘留癌細胞,讓無進展生存期延長?手術、化療、放療這些方式已經派不上用場,李先生在朋友的介紹下開始瞭解免疫治療技術,並最終選擇了清華大學免疫學張明徽教授團隊研發的vNKT免疫細胞療法。
✔ 李先生系統化療和局部治療已完成,當前腫瘤負荷已降低,正是清除微小殘留病灶的最佳窗口期。
✔ 李先生的腸癌類型對PD-1/PD-L1抑制劑幾乎無效,傳統免疫治療獲益有限。
✔ vNKT細胞是一類兼具NK細胞殺傷力與T細胞特異性的雙重抗腫瘤效應免疫細胞,不僅能夠直接殺傷癌細胞,還會調節腫瘤組織內部的免疫微環境。它在清除微小殘留病灶、延緩復發方面具有很大潛力。
實驗條件:有vNKT細胞存在的情況下,經過16個小時,近乎所有B16腫瘤細胞被殺死!
2025年10月李先生進入vNKT細胞治療,目前已完成3療程,腫瘤標誌物趨於穩定,影像學報告未出現新發病灶,整體病情平穩。
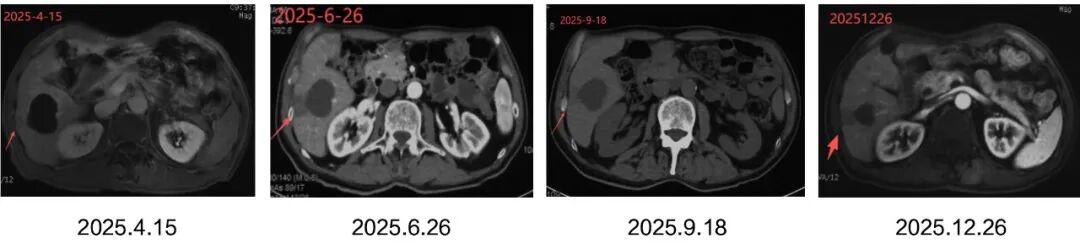
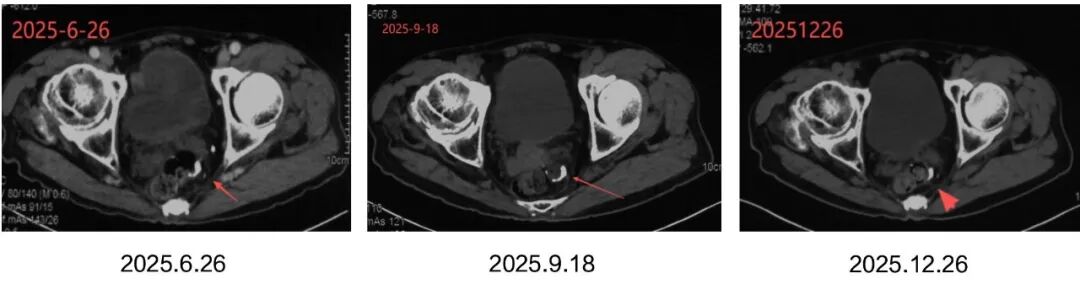
在現代腫瘤治療中,無瘤並不等於無風險,有時候看不見的敵人才是最難防的。vNKT免疫細胞治療正在成為癌症患者長久治癒的一種重要鞏固策略,它追求的不是讓腫瘤縮小,而是在腫瘤尚未捲土重來之前,提前布防、清除殘敵。這不僅是治療的延續,更是對長期生存的主動管理。
如有任何關於癌症術後免疫管理的問題,可以給張教授團隊留言。

參考文獻:
[1]Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020[J].CA Cancer J Clin, 2020, 70(1): 7-30. DOI:10.3322/caac.21590.
[2]Cohen R, Raeisi M, Chibaudel B, et al. Prognostic value of liver metastases in colorectal cancer treated by systemic therapy: An ARCAD pooled analysis[J]. Eur J Cancer, 2024,207:114160. DOI: 10.1016/j.ejca.2024.114160.
[3]Vibert E, Canedo L, Adam R. Strategies to treat primary unresectable colorectal liver metastases[J]. Semin Oncol,2005, 32(6 Suppl 8): 33-39. DOI: 10.1053/j. seminoncol.2005.07.015.
[4]de Jong MC, Pulitano C, Ribero D, et al. Rates and patterns of recurrence following curative intent surgery for colorectal liver metastasis: an international multiinstitutional analysis of 1669 patients[J]. Ann Surg, 2009,250(3):440-448. DOI: 10.1097/SLA.0b013e3181b4539b.
[5]Margonis GA, Sergentanis TN, Ntanasis-Stathopoulos I, et al. Impact of Surgical Margin Width on Recurrence and Overall Survival Following R0 Hepatic Resection of Colorectal Metastases: A Systematic Review and Metaanalysis[J]. Ann Surg, 2018, 267(6): 1047-1055. DOI:10.1097/SLA.0000000000002552.
[6]Giuliante F, Ardito F, Vellone M, et al. Role of the surgeon as a variable in long-term survival after liver resection for colorectal metastases[J]. J Surg Oncol, 2009, 100(7):538-545. DOI: 10.1002/jso.21393.
[7]Padmanabhan C, Nussbaum DP, D'Angelica M. Surgical Management of Colorectal Cancer Liver Metastases[J].Surg Oncol Clin N Am, 2021,30(1):1-25. DOI: 10.1016/j.soc.2020.09.002.
[8]Morris VK, Kennedy EB, Baxter NN, et al. Treatment of Metastatic Colorectal Cancer: ASCO Guideline[J]. J Clin Oncol, 2023,41(3):678-700. DOI: 10.1200/JCO.22.01690.
點擊查看往期案例