關於樂和
乐于心,和与众,与己乐,与人和; 心宽念纯,百病无生。

癌症患者最難熬的就是前5年,它就像一道門檻,跨過去就意味著新生。但很多人並不清楚這5年該如何順利度過,全憑運氣嗎?顯然不是!
今天我們就來看看這位術後僅9個月就發現轉移的肺癌患者的經歷,原來這一切都不是隨機發生,很多高危風險早早就已有跡可循,只是你沒看到!
2024年初,58歲的王先生發現自己咳嗽、咳痰總不好,前前後後持續了一個多月,到了5月份他決定還是到醫院查查怎麼回事。

不查不知道,胸部CT發現左肺下葉腫塊佔位灶,而且個頭還不小,較大截面有6.1cmx4.8cm。
於是王先生當月就做了左下肺葉切除術、淋巴結清掃術、肋間神經阻滯術。
○左肺下葉見差分化腺癌,部分區域伴神經內分泌分化。
○淋巴結轉移,發現左喉返神經旁淋巴結2/3枚見癌轉移,其餘區域淋巴結無轉移。
○未見明確脈管內見栓,支氣管切端陰性,分期考慮ⅡB-ⅢA期。
○免疫組化:腫瘤細胞:CK7(部分+),NapsinA(+),TTF-1(+),CK20(),P40(-),P63(-),CK5/6(-),Syna(少許+),CD56(+),NKX3.1(-),Ki-67(約40%-70%不等)。
術後2024年6月~8月,為了預防轉移復發,王先生又跟進了培美曲塞+順鉑化療,但僅做了3週期就被叫停,因為他的肌酐已經高到179μmol/L,無法耐受化療。
化療進行不下去,王先生想試試有沒有靶向藥和免疫藥可用,但基因檢測沒有突變,PD-L1檢測結果<1%,評估結果陰性,靶向藥和免疫檢查點藥物這兩個強有力的“後手”也走不通。
至此,王先生感覺他的肺癌治療之路能走的已經都走了,更何況分期不算太晚,應該問題不大。
但讓人沒想到的是病情失守來得如此快,2025年2月,王先生術後9個月復查胸部增強CT,又在縱隔內2R區發現了淋巴結腫大,活檢穿刺證實低分化腺癌轉移Ki-67(+,約70%)。
這個問題其實早有科研人員為非小細胞肺癌患者總結出了復發轉移的時間規律,一項針對T1-T3a、N0-N2期非小細胞肺癌術後患者的研究發現,術後9個月左右是復發轉移風險第一個峰值,也是風險最高的階段,之後風險就會逐步下降,到術後24個月左右迎來第二波復發轉移高峰,之後風險繼續回落,直到術後第4年,再出現第三波復發轉移高峰。[1]
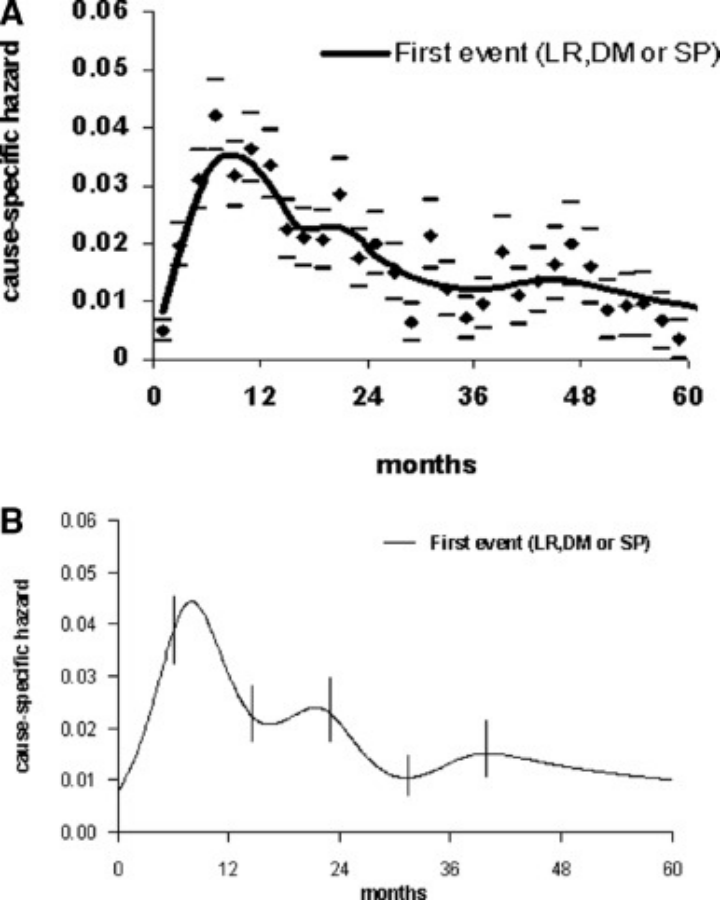
王先生肺癌術後9個月復發轉移,踩中了風險最高的階段,這可不是他運氣不好,其實風險早已有跡可循,在這裡也給大家提個醒。
1、分化差
腫瘤不只看體積大小,它的分化程度同樣重要。低分化的癌細胞分裂能力、變異能力、自我修復能力、抗化療放療能力都比高分化癌細胞更強。
神經內分泌分化也是一個狠角色,它長得快、跑得早、難對付。
王先生的Ki-67指數高達70%,意味著檢測的腫瘤組織標本中約70%的癌細胞處於活躍分裂狀態,正在瘋狂複製,這種速度有時就連常規化療都追不上。
2、淋巴結轉移/脈管癌栓
手術切除了原發病灶,但不代表就消除了所有隱患,淋巴結轉移和脈管癌栓就是癌症復發的重要隱患。
淋巴系統和血液系統是癌細胞擴散到全身的重要通道,當出現淋巴結轉移和脈管癌栓則提示腫瘤生物學侵襲性強,預示著癌細胞進入全身播散階段,需要加強術後輔助治療來圍剿殘留病灶。
3、治療手段受限
在臨床中經常能看到像王先生一樣因化療副作用太大終止治療;無法匹配突變基因吃不了靶向藥;以及PD-L1表達陰性,無法從免疫檢查點抑制劑治療中獲益的的患者。
這意味著患者將失去一種或幾種高效的抗癌武器,對殘留癌細胞的清除和轉移復發風險的降低也將大打折扣,治癒概率變得不確定。
王先生復發轉移後再次開啓治療之路,2025年3月換了白蛋白紫杉醇+卡鉑+貝伐珠單抗的新化療方案再次嘗試,但依然出現了骨髓抑制,藥量減半後也僅完成了2週期就不得不放棄。
2025年5月至6月,為瞭解決局部轉移病灶他又接受了碳離子放射治療。
全身性治療的缺失與虎視眈眈的高風險因素,讓王先生和家人再也坐不住了。如何彌補這部分的治療漏洞,他找到了清華大學張明徽教授團隊。
經張明徽教授的樂和新醫團隊分析:
① 王先生腫瘤的低分化、神經內分泌分化、Ki-67(+,約70%)、淋巴結轉移等指標讓他不得不被划為復發轉移高危人群。術後輔助治療不僅要做,強度還要足夠。
② 王先生在治療過程中化療不耐受,靶向藥無靶點,PD-L1獲益可能性低,常規全身性治療手段乏力,急需新的輔助治療手段介入,vNKT細胞治療序貫使用獲益證據充分。
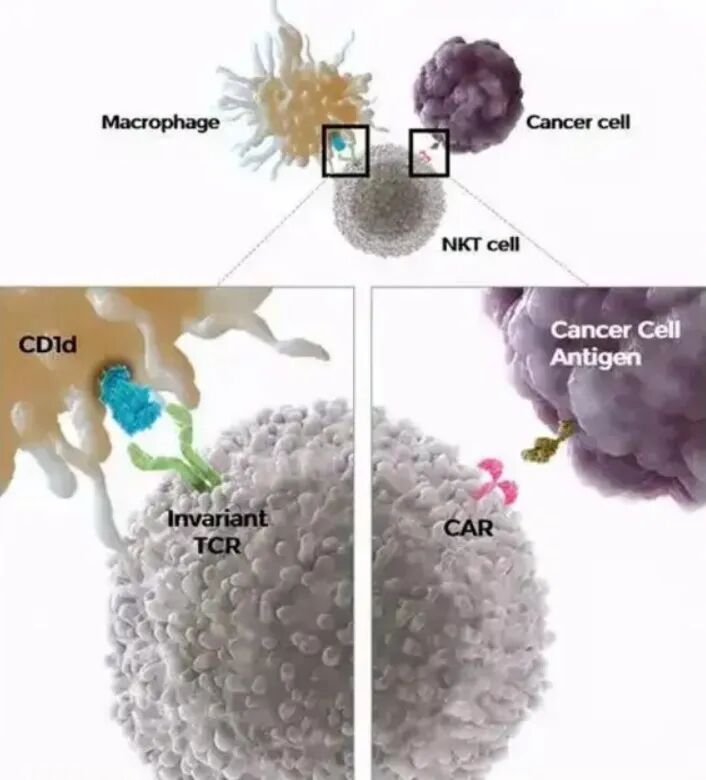
vNKT細胞治療作為一種過繼性細胞免疫療法屬於全身性治療,它不依賴PD-L1表達,也無需靶點匹配,而是通過分離出健康人體內本就有的免疫細胞,經過體外改造擴增,使其具有更強的抗癌能力,再回輸給患者。由於vNKT細胞在體內的數量非常少,這種擴增後-活化-回輸的方式相當於為給身體請外援。
實驗條件:有vNKT細胞存在的情況下,經過16個小時,近乎所有B16腫瘤細胞被殺死!
vNKT細胞是一種細胞表面既有T細胞受體TCR,又有NK細胞受體的特殊T細胞亞群,它兼具非特異性和特異性識別腫瘤細胞的雙重能力,可以非常快速地殺傷腫瘤細胞。同時調節腫瘤組織內部的免疫微環境,殺傷抑制性免疫細胞MDSCs,打破腫瘤的免疫逃逸也是它的特長。對於重建正常免疫系統、清除殘留癌細胞、進一步預防復發轉移具有獨特優勢。
③ 王先生對化療高度不耐受,安全性成為他選擇其他治療方式的重要條件,與傳統的化療和放療相比,vNKT細胞治療的副作用極小,患者更容易耐受。
④ 目前王先生已切除原發病灶,轉移後碳離子放射治療解決了局部病灶,降低瘤負荷後正是介入vNKT細胞治療的好時機。
聽了張教授團隊的分析,王先生對vNKT細胞充滿期待,於是2025年6月進入治療,經過8療程後,通過影像學和腫瘤標誌物檢查可以看到,淋巴結增大的速度開始放緩,病灶逐漸穩定下來,腫瘤標誌物也回落到正常水平。
更讓人驚喜的是,vNKT回輸後王先生發現自己的體質變好了,感冒發燒的次數比過去明顯少了,身上也有力氣了,就連頭髮都開始變黑,皮膚也變細膩,身體又進入了良性循環。
王先生的經歷再次印證了“復發轉移並不是靠運氣,轉移復發早已給過提示,那些“看不見”的殘留敵人從未真正離開”。
手術刀可以剔除肉眼可見的腫瘤,但總有極少數狡猾的癌細胞能躲過常規治療的追殺,它們隱藏、偽裝,靜待時機捲土重來。
術後9個月的平靜期並不是治癒的證明,而是暴風雨前的寧靜。
對抗癌症從來不是一場靠運氣的博弈,而是一場靠科學洞察先機的持久戰。真正笑到最後的是那些敢於直面“高危風險”主動出擊的人。精准的監測和前沿的治療,才是幫助患者跨越5年門檻最堅實的底氣。


參考來源:
[1]Romano Demicheli, Marco Fornili, Federico Ambrogi, Kristin Higgins, Jessamy A. Boyd, Elia Biganzoli, Chris R. Kelsey,Recurrence Dynamics for Non–Small-Cell Lung Cancer: Effect of Surgery on the Development of Metastases,Journal of Thoracic Oncology,2012,7(4):723-730. DOI:10.1097/JTO.0b013e31824a9022.
點擊查看往期案例

