關於樂和
乐于心,和与众,与己乐,与人和; 心宽念纯,百病无生。

疫苗通常是指利用抗原類物質接種到體內,激活人體的免疫系統,實現對該病原體的免疫清除,從而保護人體健康。疫苗是人類主動對抗疾病的有力武器,根據應用目的可分為預防性疫苗和治療性疫苗兩大類。
傳染病疫苗是預防性疫苗的典型代表。200多年前,英國鄉村醫生愛德華・詹納利用牛痘接種預防天花,開創了疫苗接種、消除病原體、保護人體健康的干預模式。疫苗接種可使人體產生針對相應病原體的長期免疫保護力,世界衛生組織(WHO)通過在全球推行牛痘接種,於1980年消滅了天花。目前我國對新生嬰兒均實施計劃免疫,預防脊髓灰質炎、白喉、百日咳、破傷風、麻疹及結核病等傳染病。由此可見,疫苗接種技術已相對成熟,成為防控傳染病最經濟、最有效的手段。
癌症疫苗是一類以制備的腫瘤抗原為基礎,通過激活腫瘤患者機體自身免疫系統,誘導其產生對腫瘤細胞的特異性免疫應答,最終實現對腫瘤細胞的識別與殺傷的免疫治療制劑。癌症疫苗的抗原種類較多,包括靶向腫瘤異常表達的通用腫瘤相關抗原疫苗(如癌胚抗原CEA 疫苗)、以完整腫瘤細胞為抗原源的全腫瘤細胞疫苗等。其中,通過下一代基因測序(NGS)檢測患者腫瘤突變而制備的個體化新抗原疫苗,尤其受到關注。研究表明,個體化新抗原癌症疫苗(蛋白短肽或 mRNA 型)可在黑色素瘤、胰腺癌等腫瘤患者體內,誘導出強效、持久的特異性抗腫瘤T細胞應答。目前已有多款個體化新抗原癌症疫苗進入臨床Ⅱ/Ⅲ期研究,展現出良好的腫瘤治療應用前景。
對於人體而言,T細胞介導的免疫保護是最重要的抗腫瘤免疫功能之一,那麼癌症疫苗能否在人體內誘導出長達6年的持久抗腫瘤T細胞免疫保護作用?
▶▶研究是怎麼做的?
德國學者2025年發表在《自然》(Nature)上的一項研究,為這一問題提供了答案——該研究探索了個體化mRNA疫苗在三陰性乳腺癌輔助治療中的應用效果(Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC,Nature,2025)。

三陰性乳腺癌(TNBC)是一種高度異質性、惡性程度較高的乳腺癌亞型,其雌激素受體(ER)、孕激素受體(PR)和人表皮生長因子受體2(HER2)均為陰性,約佔所有乳腺癌的 15%~20%。儘管目前 TNBC 的治療已有PD-1/PD-L1抑制劑聯合化療、BRCA突變患者的PARP抑制劑精准治療等方案,但該亞型仍因侵襲性強、增殖快、易發生早期遠處轉移,且缺乏明確靶向靶點,成為乳腺癌治療的難點。不過TNBC存在基因組不穩定性高的生物學特徵,腫瘤細胞內可表達大量突變蛋白,呈現出免疫原性較強的特點,因此成為採用新抗原癌症疫苗進行個體化治療的理想對象。
該研究的臨床試驗註冊號為NCT02316457,採用TNBC-MERIT(突變組工程化RNA免疫治療)臨床治療方案,通過個體化疫苗制備、臨床接種、多維度免疫檢測和長期臨床隨訪的研究策略開展試驗。
研究共招募15例經組織學確診的早期浸潤性TNBC患者,入組標準為:術後1年內完成標準新輔助/輔助治療、腫瘤可識別出至少5個新抗原、無腫瘤復發。其中14例患者完成方案治療,納入最終治療效果評估。
個體化mRNA 癌症疫苗的制備過程,與新冠疫苗等預防性病原體疫苗截然不同。研究人員先對患者腫瘤組織及外周血單核細胞進行基因測序,結合生物信息學算法預測能誘導T細胞免疫的腫瘤新抗原;再將篩選出的腫瘤新抗原基因序列,與可增強T細胞抗原提呈的分泌信號肽、人類白細胞抗原I類分子轉運域(MITD)進行組裝;最後將該mRNA用脂質體納米粒(LPX)包裝,構建出適用於每位患者的個體化mRNA癌症疫苗。這一制備過程的平均耗時為69天(34~125天),且需為每位患者單獨制備。
癌症疫苗的接種方式也與預防性疫苗不同,預防性疫苗多采用皮下、皮內或口服接種,而治療性癌症疫苗需結合患者的臨床治療方案實施:患者先接受外科手術、化療或放療等干預治療,再通過靜脈注射接種個體化mRNA癌症疫苗。本研究中,患者共接受8劑個體化疫苗接種,前6劑每周1次,後2劑每2周1次,最後1劑在第64天完成。14例患者中,3例先接種基於腫瘤相關抗原(TAA)的橋接疫苗,再進行14.4μg至50μg的劑量遞增接種以驗證安全性;經安全評估後,其餘11例直接採用50μg的治療目標劑量。
對於干預性臨床試驗,患者的安全性是首要評價指標。本研究中,患者接種疫苗後出現的治療相關不良事件,絕大多數為1級或2級,如發熱、頭痛、寒戰和疲勞,且這些症狀多在接種後1~3天出現,通常1天內即可自行緩解。僅1例患者因出現3級低血壓、2級惡心等不良事件,在接種3劑後停藥。這一結果表明,該癌症疫苗的整體使用安全性良好。
癌症疫苗的抗腫瘤效應主要通過激活患者體內的T細胞功能實現,因此研究人員採用IFN-γ酶聯免疫斑點(ELISpot)法、T細胞受體(TCR)測序等方法,評估患者接種後的免疫狀態,重點檢測T細胞的免疫功能。結果顯示,個體化mRNA癌症疫苗可在患者體內誘導出強效、多表位的新抗原特異性T細胞應答:所有14例患者均誘導出針對疫苗新抗原的T細胞應答,9例患者對至少5個新抗原產生應答,86%的患者可通過體外 ELISpot 檢測到新抗原特異性T細胞應答;疫苗誘導的T細胞應答以從頭應答為主,41個突變靶點在接種前未檢測到T細胞應答,接種後可明確檢測,僅2個新抗原存在基線 T 細胞應答,並被疫苗進一步擴增。
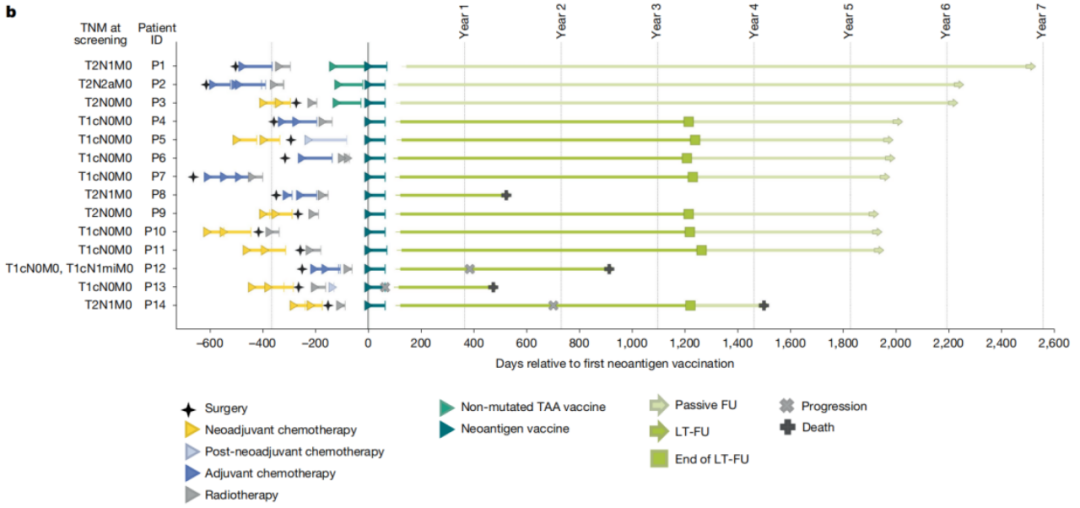
同時研究還發現,疫苗誘導的T細胞應答具有長期持久性,且激活的T細胞表型、功能多樣。疫苗誘導的多新抗原T細胞應答在接種後雖出現短暫收縮,但仍能在1~3.5 年內維持高水平;即便無疫苗加強針,部分患者體內的新抗原特異性CD8+T細胞在接種後6年,仍可在外周血中檢測到。疫苗誘導的CD8+T細胞主要為效應記憶T細胞和終末分化效應記憶T細胞群體,同時還存在乾細胞樣記憶細胞表型的T細胞亞群,尤其在P1患者體內,這群共表達TCF-1和IL-7Rα 的乾性記憶T細胞,在疫苗接種6年後仍可在外周血中檢測到。
▶▶效果如何?
那麼這款癌症疫苗的治療效果如何?該試驗的中位隨訪期長達5年(62個月,區間15~80個月),14名患者中有11名未出現任何復發跡象;其中P8患者在最後一劑疫苗接種15個月後死於未知原因,生前未出現腫瘤復發。這一高獲益結果,證實了個體化mRNA癌症疫苗治療TNBC的有效性。
該試驗雖取得了較好的治療效果,但也暴露了腫瘤治療的複雜性與挑戰:有3例患者在治療期間出現疾病復發。其中,疫苗誘導T細胞應答最弱的P14患者復發後,接受抗PD-1治療實現完全緩解,但後續發生全身復發並死亡;P13患者的原發腫瘤細胞表面,與CD8+T細胞應答相關的人類白細胞I類抗原分子表達水平低,復發腫瘤中該類分子幾乎完全缺失,抗原呈遞通路關鍵基因(如B2M、HLA家族基因)表達下調,即便患者體內有疫苗誘導的功能性T細胞浸潤,腫瘤仍通過抗原呈遞障礙實現免疫逃逸;P12患者為BRCA1突變陽性的雙側TNBC,癌症疫苗的設計基於右側乳腺腫瘤的測序結果,但其復發源於左側乳腺獨立進化的原發腫瘤,該腫瘤的突變特徵與疫苗靶向的腫瘤完全無關,且復發腫瘤中未檢測到疫苗誘導的新抗原特異性T細胞。這些治療失敗的案例表明,腫瘤治療仍需探索新方案,尤其是聯合治療方案。
綜上所述,該研究系統探索了個體化新抗原mRNA癌症疫苗的制備、腫瘤患者的免疫接種,並分析了其安全性、體內特異性T細胞應答水平及治療效果。研究證實,這類治療性個體化新抗原mRNA 疫苗具有較強的免疫原性,可在接受手術及新輔助/輔助治療後的早期TNBC患者體內,激活持久的CD8+T細胞免疫應答,且臨床可行性良好、不良反應可控、安全性較高。同時研究也發現,部分患者會因腫瘤抗原免疫原性差異、抗原提呈功能障礙等免疫逃逸機制,影響疫苗治療效果,這為後續優化疫苗治療策略提供了重要啓示。