关于乐和
乐于心,和与众,与己乐,与人和; 心宽念纯,百病无生。

疫苗通常是指利用抗原类物质接种到体内,激活人体的免疫系统,实现对该病原体的免疫清除,从而保护人体健康。疫苗是人类主动对抗疾病的有力武器,根据应用目的可分为预防性疫苗和治疗性疫苗两大类。
传染病疫苗是预防性疫苗的典型代表。200多年前,英国乡村医生爱德华・詹纳利用牛痘接种预防天花,开创了疫苗接种、消除病原体、保护人体健康的干预模式。疫苗接种可使人体产生针对相应病原体的长期免疫保护力,世界卫生组织(WHO)通过在全球推行牛痘接种,于1980年消灭了天花。目前我国对新生婴儿均实施计划免疫,预防脊髓灰质炎、白喉、百日咳、破伤风、麻疹及结核病等传染病。由此可见,疫苗接种技术已相对成熟,成为防控传染病最经济、最有效的手段。
癌症疫苗是一类以制备的肿瘤抗原为基础,通过激活肿瘤患者机体自身免疫系统,诱导其产生对肿瘤细胞的特异性免疫应答,最终实现对肿瘤细胞的识别与杀伤的免疫治疗制剂。癌症疫苗的抗原种类较多,包括靶向肿瘤异常表达的通用肿瘤相关抗原疫苗(如癌胚抗原CEA 疫苗)、以完整肿瘤细胞为抗原源的全肿瘤细胞疫苗等。其中,通过下一代基因测序(NGS)检测患者肿瘤突变而制备的个体化新抗原疫苗,尤其受到关注。研究表明,个体化新抗原癌症疫苗(蛋白短肽或 mRNA 型)可在黑色素瘤、胰腺癌等肿瘤患者体内,诱导出强效、持久的特异性抗肿瘤T细胞应答。目前已有多款个体化新抗原癌症疫苗进入临床Ⅱ/Ⅲ期研究,展现出良好的肿瘤治疗应用前景。
对于人体而言,T细胞介导的免疫保护是最重要的抗肿瘤免疫功能之一,那么癌症疫苗能否在人体内诱导出长达6年的持久抗肿瘤T细胞免疫保护作用?
▶▶研究是怎么做的?
德国学者2025年发表在《自然》(Nature)上的一项研究,为这一问题提供了答案——该研究探索了个体化mRNA疫苗在三阴性乳腺癌辅助治疗中的应用效果(Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC,Nature,2025)。

三阴性乳腺癌(TNBC)是一种高度异质性、恶性程度较高的乳腺癌亚型,其雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)均为阴性,约占所有乳腺癌的 15%~20%。尽管目前 TNBC 的治疗已有PD-1/PD-L1抑制剂联合化疗、BRCA突变患者的PARP抑制剂精准治疗等方案,但该亚型仍因侵袭性强、增殖快、易发生早期远处转移,且缺乏明确靶向靶点,成为乳腺癌治疗的难点。不过TNBC存在基因组不稳定性高的生物学特征,肿瘤细胞内可表达大量突变蛋白,呈现出免疫原性较强的特点,因此成为采用新抗原癌症疫苗进行个体化治疗的理想对象。
该研究的临床试验注册号为NCT02316457,采用TNBC-MERIT(突变组工程化RNA免疫治疗)临床治疗方案,通过个体化疫苗制备、临床接种、多维度免疫检测和长期临床随访的研究策略开展试验。
研究共招募15例经组织学确诊的早期浸润性TNBC患者,入组标准为:术后1年内完成标准新辅助/辅助治疗、肿瘤可识别出至少5个新抗原、无肿瘤复发。其中14例患者完成方案治疗,纳入最终治疗效果评估。
个体化mRNA 癌症疫苗的制备过程,与新冠疫苗等预防性病原体疫苗截然不同。研究人员先对患者肿瘤组织及外周血单核细胞进行基因测序,结合生物信息学算法预测能诱导T细胞免疫的肿瘤新抗原;再将筛选出的肿瘤新抗原基因序列,与可增强T细胞抗原提呈的分泌信号肽、人类白细胞抗原I类分子转运域(MITD)进行组装;最后将该mRNA用脂质体纳米粒(LPX)包装,构建出适用于每位患者的个体化mRNA癌症疫苗。这一制备过程的平均耗时为69天(34~125天),且需为每位患者单独制备。
癌症疫苗的接种方式也与预防性疫苗不同,预防性疫苗多采用皮下、皮内或口服接种,而治疗性癌症疫苗需结合患者的临床治疗方案实施:患者先接受外科手术、化疗或放疗等干预治疗,再通过静脉注射接种个体化mRNA癌症疫苗。本研究中,患者共接受8剂个体化疫苗接种,前6剂每周1次,后2剂每2周1次,最后1剂在第64天完成。14例患者中,3例先接种基于肿瘤相关抗原(TAA)的桥接疫苗,再进行14.4μg至50μg的剂量递增接种以验证安全性;经安全评估后,其余11例直接采用50μg的治疗目标剂量。
对于干预性临床试验,患者的安全性是首要评价指标。本研究中,患者接种疫苗后出现的治疗相关不良事件,绝大多数为1级或2级,如发热、头痛、寒战和疲劳,且这些症状多在接种后1~3天出现,通常1天内即可自行缓解。仅1例患者因出现3级低血压、2级恶心等不良事件,在接种3剂后停药。这一结果表明,该癌症疫苗的整体使用安全性良好。
癌症疫苗的抗肿瘤效应主要通过激活患者体内的T细胞功能实现,因此研究人员采用IFN-γ酶联免疫斑点(ELISpot)法、T细胞受体(TCR)测序等方法,评估患者接种后的免疫状态,重点检测T细胞的免疫功能。结果显示,个体化mRNA癌症疫苗可在患者体内诱导出强效、多表位的新抗原特异性T细胞应答:所有14例患者均诱导出针对疫苗新抗原的T细胞应答,9例患者对至少5个新抗原产生应答,86%的患者可通过体外 ELISpot 检测到新抗原特异性T细胞应答;疫苗诱导的T细胞应答以从头应答为主,41个突变靶点在接种前未检测到T细胞应答,接种后可明确检测,仅2个新抗原存在基线 T 细胞应答,并被疫苗进一步扩增。
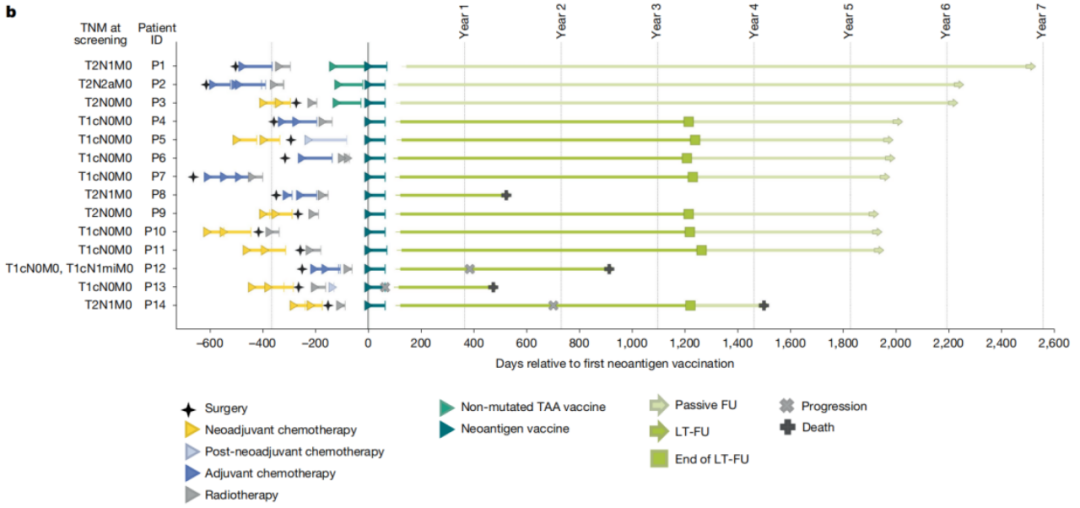
同时研究还发现,疫苗诱导的T细胞应答具有长期持久性,且激活的T细胞表型、功能多样。疫苗诱导的多新抗原T细胞应答在接种后虽出现短暂收缩,但仍能在1~3.5 年内维持高水平;即便无疫苗加强针,部分患者体内的新抗原特异性CD8+T细胞在接种后6年,仍可在外周血中检测到。疫苗诱导的CD8+T细胞主要为效应记忆T细胞和终末分化效应记忆T细胞群体,同时还存在干细胞样记忆细胞表型的T细胞亚群,尤其在P1患者体内,这群共表达TCF-1和IL-7Rα 的干性记忆T细胞,在疫苗接种6年后仍可在外周血中检测到。
▶▶效果如何?
那么这款癌症疫苗的治疗效果如何?该试验的中位随访期长达5年(62个月,区间15~80个月),14名患者中有11名未出现任何复发迹象;其中P8患者在最后一剂疫苗接种15个月后死于未知原因,生前未出现肿瘤复发。这一高获益结果,证实了个体化mRNA癌症疫苗治疗TNBC的有效性。
该试验虽取得了较好的治疗效果,但也暴露了肿瘤治疗的复杂性与挑战:有3例患者在治疗期间出现疾病复发。其中,疫苗诱导T细胞应答最弱的P14患者复发后,接受抗PD-1治疗实现完全缓解,但后续发生全身复发并死亡;P13患者的原发肿瘤细胞表面,与CD8+T细胞应答相关的人类白细胞I类抗原分子表达水平低,复发肿瘤中该类分子几乎完全缺失,抗原呈递通路关键基因(如B2M、HLA家族基因)表达下调,即便患者体内有疫苗诱导的功能性T细胞浸润,肿瘤仍通过抗原呈递障碍实现免疫逃逸;P12患者为BRCA1突变阳性的双侧TNBC,癌症疫苗的设计基于右侧乳腺肿瘤的测序结果,但其复发源于左侧乳腺独立进化的原发肿瘤,该肿瘤的突变特征与疫苗靶向的肿瘤完全无关,且复发肿瘤中未检测到疫苗诱导的新抗原特异性T细胞。这些治疗失败的案例表明,肿瘤治疗仍需探索新方案,尤其是联合治疗方案。
综上所述,该研究系统探索了个体化新抗原mRNA癌症疫苗的制备、肿瘤患者的免疫接种,并分析了其安全性、体内特异性T细胞应答水平及治疗效果。研究证实,这类治疗性个体化新抗原mRNA 疫苗具有较强的免疫原性,可在接受手术及新辅助/辅助治疗后的早期TNBC患者体内,激活持久的CD8+T细胞免疫应答,且临床可行性良好、不良反应可控、安全性较高。同时研究也发现,部分患者会因肿瘤抗原免疫原性差异、抗原提呈功能障碍等免疫逃逸机制,影响疫苗治疗效果,这为后续优化疫苗治疗策略提供了重要启示。